互聯網金融作為金融與科技融合的產物,近年來深刻改變了傳統金融服務模式。本文基于40張PPT的框架,系統梳理互聯網金融的核心概念、發展歷程、主要模式以及金融信息咨詢的關鍵作用,幫助讀者全面理解這一領域的動態與趨勢。
一、互聯網金融概述
互聯網金融是指利用互聯網技術和移動通信技術實現資金融通、支付、投資和信息中介服務的新型金融業務模式。其特點包括高效便捷、低成本、覆蓋面廣,并推動了金融普惠化。從早期的在線支付到如今的智能投顧,互聯網金融已滲透到借貸、保險、財富管理等多個細分領域。
二、互聯網金融的主要模式
- 支付結算:如支付寶、微信支付等第三方支付平臺,簡化了交易流程。
- 網絡借貸:P2P網貸和眾籌平臺為個人和小微企業提供了融資渠道。
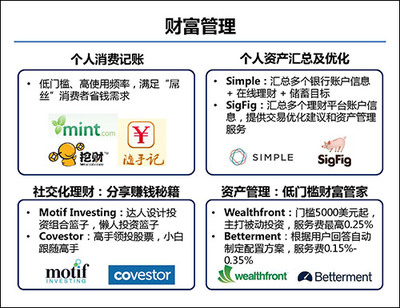
- 互聯網理財:通過平臺銷售基金、保險等產品,降低了投資門檻。
- 數字貨幣與區塊鏈:比特幣和分布式賬本技術正重塑金融基礎設施。
- 金融科技(FinTech):大數據、人工智能等技術應用于風險控制和客戶服務。
三、金融信息咨詢的重要性
金融信息咨詢是互聯網金融生態中的關鍵環節,它為用戶提供市場分析、產品比較、風險評估和投資建議等服務。在信息爆炸的時代,專業的咨詢能幫助用戶規避風險、優化決策。例如,通過數據挖掘和算法模型,咨詢平臺可提供個性化理財方案,提升用戶體驗。
四、發展趨勢與挑戰
未來,互聯網金融將更注重合規與安全,各國監管政策逐步完善。同時,AI和區塊鏈的深入應用將推動服務智能化。風險如數據隱私、網絡欺詐等仍需警惕。金融信息咨詢需加強透明度,以建立用戶信任。
五、總結
互聯網金融不僅是技術革新,更是金融民主化的體現。結合40張PPT的詳細解析,我們可以清晰看到其多元化模式及信息咨詢的價值。隨著技術演進,這一領域將繼續演化,為用戶創造更多機遇。